- 抑制剂 (9639)
- 试剂 (2801)
- elisa试剂盒 (2901)
- ATCC细胞 (1335)
- 标准品 (660)
- 培养基 (953)
- USP标准品 (1815)
- ELISA检测试剂盒 (6995)
- 抗体 (4401)
- 标准品、对照品 (1858)
- RNA/DNA提取 (1127)
- ELISA Kit (3138)
- 原代细胞 (297)
- 标准品 (323)
- PCR检测试剂盒 (1273)
- 德国DRG试剂盒 (264)
- 生命科学 (654)
- 生化检测试剂盒 (445)
- 标准物质 (1102)
- 生化试剂 (2070)
- 进口品牌 (221)
- 代理品牌 (27)
- 生物碱 (493)
- 黄酮 (521)
- 查尔酮 (50)
- 氧杂蒽酮 (178)
- 香豆素 (169)
- 木脂素 (67)
- 苯丙素 (96)
- 药物杂质及中间体 (825)
- 其它天然产物 (153)
- 蒽醌 (26)
- 其它醌类 (44)
- 甾体 (166)
- 二萜 (507)
- 其它萜类 (56)
- 环烯醚萜 (135)
- 倍半萜 (395)
- 中药对照品 (1675)
- 其它酚类 (567)
- 三萜 (476)
- 荧光定量试剂盒 (2052)
- 细胞库 (824)
- 耗材和仪器 (1)
- 细胞生物学试剂 (2716)
- 进口抗体 (2253)
- ELISA Kit (2843)
- PCR基因检测试剂盒 (2215)
- 植物标准品 (1069)
- 细胞因子 (1071)
- 检测试剂盒 (4149)
- 科研抗体 (17457)
- 蛋白 (2387)
- 细胞 (918)
- 其他分类 (15)
原代细胞常用纯化方法步骤
发布时间:2024-09-24 10:00 | 点击次数:2424
原代细胞人工纯化是利用人为手段造成对某一细胞生长有利的环境条件,抑制其他细胞的生长从而达到纯化细胞的目的。在人工纯化的实践中,科学家们不断探索着更为精细与高效的方法。他们利用现代生物技术,如基因编辑技术,精准地调控目标细胞的生长基因表达,同时设计特定的抑制剂,针对非目标细胞进行精准打击,从而实现更为彻底的细胞纯化。这种方法不仅提高了纯化的效率,还大大降低了对细胞活性的损伤,确保了纯化后细胞的健康与活力。
1、细胞时间差酶消化法:
酶消化法是比较常用的纯化方法,不仅对贴壁细胞可行,能利用上皮细胞和成纤维细胞对胰蛋白酶的耐受性不同,是两者分开,达到纯化的目的;另外对贴壁细胞与半贴壁细胞及黏附细胞间的分离纯化也是十分有效的。
两者在胰蛋白酶的作用下,由于成纤维细胞先脱壁,而上皮细胞要消化相当长的时间才脱壁,特别是在原代细胞初次传代和早期传代中两种差别尤为明显,故可采用多次差别消化方法将上皮细胞和成纤维细胞分开,方法步骤如下:
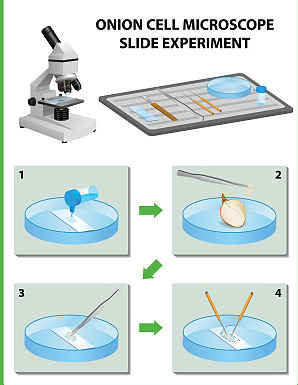
采用常规消化传代方式将0.25%胰蛋白酶注入培养瓶内两次,每次加1ml(25ml培养瓶),来回轻摇1-2次,使胰蛋白酶流过所有细胞表面,然后倒掉。
盖好瓶塞,将培养瓶放在倒置显微镜下观察,发现成纤维细胞变园,部分脱落,立即加入2ml有血清的培养基终止消化。
用弯头吸管轻轻吹打成纤维细胞生长区域(可事先在镜下用记号笔在培养瓶上划出记号)。吹打时不要用力,也不要吹打上皮细胞生长区域。吹打结束后,再用少量培养基漂洗一遍,然后加入适量培养基于瓶内继续培养,也可重复上述操作再进行一次。
隔几日后或下次传代时,再进行上述操作,进过几次处理,就可将成纤维细胞去除或者将两者分开。
2、细胞培养机械刮除法:
原代培养时,如果上皮细胞和成纤维细胞分为区成混杂生长,每种细胞都以小片或区域性分布的方式生长在瓶壁上。可采用机械的方法去除不需要的细胞区域而保留需要的细胞区域,其方法步骤如下 :
将要纯化细胞的培养瓶,在净化室内放在倒置显微镜监视下进行操作。
用硅橡胶刮子在不需要生长的细胞区域推划,使细胞悬浮在培养基中,注意不要伤及所需细胞。
推划后用培养基冲洗振摇两次倒掉,即可将培养基加入原瓶继续培养。
数日后如发现不需要的细胞又长出,可再进行上述操作,这样反复多次可以纯化细胞。操作过程中要严格无菌操作,防止污染。
3、细胞反复贴壁法:
成纤维细胞与上皮细胞相比,其贴壁过程快,大部分细胞能在短时间内(大约10-30min)完成附着过程(但不一定完全伸展),而上皮细胞(大部分)在短时间内不能附着或附着不稳定,稍加振荡即浮起,利用此差别可以纯化细胞。
将细胞悬液接种在一个培养内(最好培养基内不含血清,此时上皮细胞贴壁更慢)静置20min。
在倒置显微镜下观察,见部分细胞贴壁,稍加摇动也不浮起时,将细胞悬液导入另一培养瓶中。
继续静置培养20min,然后重复上述操作后,即可将上皮细胞和成纤维细胞分隔开,在第一瓶和第二瓶以成纤维细胞为主,往后几瓶即以上皮细胞为主,下次传代时再按上述方法处理,就可使两者达到完全分开的目的。
4、细胞电烙筛选法:
在贴壁细胞转化时,往往在培养瓶的细胞层中会出现分散的转化灶,转化灶区域细胞密集、排列规则,有明显生长趋势,与周边未能转化的细胞有明显的区域界限,此时即可用机械刮除法取出未转化细胞,也可用电烙筛选法烫死未转化细胞而保留转化灶细胞。
原代细胞倒去原液,并用记号笔划出转化灶的区域。
用加热的微型电烙器(类似焊接用的电烙铁)将转化灶周边的细胞全部烫死,只保留转化灶细胞。在单细胞克隆筛选时,也可用此法将单个细胞周围的细胞杀死。
然后在适应性培养基中(50%是原液)继续培养,即可达到纯化的目的。
此外,随着材料科学的进步,人工培养基质也得到了极大的改进。科学家们研发出能够模拟细胞自然生长环境的智能基质,这些基质能够根据细胞的生长需求动态调整其物理性质和化学成分,为细胞提供最佳的生长条件。这种智能化的培养环境不仅促进了目标细胞的快速增殖,还进一步抑制了杂细胞的生长,使得纯化过程更加高效且易于控制。
同时,自动化与智能化技术的应用也为人工纯化带来了革命性的变化。通过集成先进的自动化设备和智能控制系统,科学家们可以实现对整个纯化过程的远程监控与精确调控,大大减轻了人工操作的负担,提高了实验的准确性和可重复性。这种高度自动化的纯化流程,不仅提高了科研效率,也为细胞治疗、药物研发等领域提供了更为可靠和稳定的细胞来源。
综上所述,人工纯化技术在不断的创新与发展中,正向着更加精准、高效、智能的方向迈进。未来,随着科学技术的不断进步,我们有理由相信,人工纯化将在更多领域展现出其独特的魅力和无限的潜力。


